马尔堡病毒疫苗在首次人体研究中显示出可喜的结果
《柳叶刀》杂志新发表的一篇论文表明,一种针对马尔堡病毒 (MARV) 的实验性疫苗是安全的,并在一项小型首次人体临床试验中诱导了免疫反应。这种疫苗由美国国立卫生研究院下属的国家过敏和传染病研究所 (NIAID) 的研究人员开发,有朝一日可能成为应对马尔堡病毒爆发的重要工具。
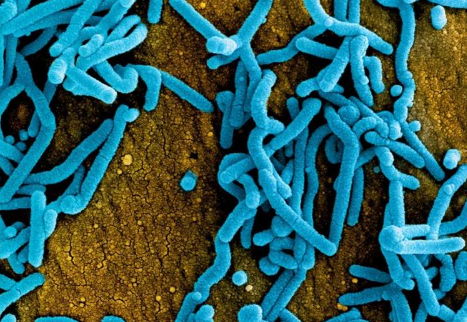
这项首次在人体中进行的第一阶段研究测试了一种实验性 MARV候选疫苗,称为 cAd3-Marburg,它是在 NIAID 的疫苗研究中心 (VRC) 开发的。这种疫苗使用一种名为 cAd3 的改良黑猩猩腺病毒,它不能再复制或感染细胞,并展示一种在 MARV 表面发现的糖蛋白,以诱导针对病毒的免疫反应。当用于 VRC 开发的研究性埃博拉病毒和苏丹病毒疫苗时,cAd3 疫苗平台在之前的临床试验中表现出良好的安全性。
MARV 是一种与埃博拉病毒属于同一家族的丝状病毒,可引起快速进展的发热性疾病,导致大部分感染者休克和死亡。许多科学家认为,当病毒从其主要动物宿主身上跳跃时,人类就会爆发 MARV 疾病,这很可能是撒哈拉以南非洲地区某些慢性感染的蝙蝠。MARV 病的症状类似于埃博拉病毒病,可能包括发烧、头痛、发冷、皮疹、腹痛、呕吐和腹泻。随着疾病的进展,患者可能会出现多器官功能障碍、精神错乱以及胃肠道或其他可能导致死亡的部位的大量出血。
除了支持性治疗外,没有针对 MARV 疾病的批准疫苗或特定疗法。虽然之前已经对一些实验性疫苗进行了测试,但没有一种疫苗被证明既高效又能提供持久保护。在最需要马尔堡疫苗的非洲地区,能够长期保护接种者的单剂量疫苗将是平息疫情的关键部分。
在这项研究中,40 名健康的成年志愿者在马里兰州银泉的沃尔特里德陆军研究所临床试验中心登记。他们接受单剂低剂量疫苗(1x1010粒子单位)或高剂量(1x1011粒子单位)。为了安全起见,志愿者参加了剂量递增计划。三名参与者接受了较低的剂量。然后,当他们在前 7 天后没有表现出严重的不良反应时,试验继续招募剩余的 17 名志愿者。相同的程序也用于较高剂量组。监测志愿者对研究疫苗的不良反应,并在 48 周内定期评估以追踪他们的免疫反应。
该试验的安全性结果令人鼓舞:没有出现严重的不良事件,实验疫苗的耐受性良好。高剂量组的一名参与者在接种疫苗后发烧,但在第二天就消退了。此外,研究性疫苗似乎对 MARV 糖蛋白产生了强烈、持久的免疫力:95% 的试验参与者在接种疫苗后表现出强烈的抗体反应,70% 的人保持这种反应超过 48 周。